Innan mosa eller baka och äta dessa läckra potatis ikväll, vad sägs om att använda dem för att lära sig lite om kemiska reaktioner först? Du kan göra detta genom att bygga en klocka som körs enbart på potatis. Ge det en go innan guffawing!
Steg
- 1Montera de objekt som behövs. Dessa listas nedan under "Du behöver".
- 2Separera de två potatisar. Varje potatis fungerar som en "galvanisk cell," frigöra elektrisk energi genom kemiska reaktioner. Ring en potatis A (eller 1), och den andra potatisen B (eller 2).
- Huvuddelen av potatisen fungerar precis som ett fall för cellen, håller allt på plats. Potatisen juice fungerar som "elektrolyt", där laddade atomer och molekyler som kallas "joner" Lös upp och kan flöda över tiden. Den utspädda fosforsyra i det ger också vätejoner för reaktionen.
- Vissa atomer (eller molekyler) lockar starkt extra elektroner och blir negativt laddade joner, som kallas lök ("An-joner"), andra är lätt fråntagen vissa elektroner och blir positivt laddade "katjoner" ("katt-joner"). Varje element attraherar elektroner med olika kraft, på grund av den varierande ansvar för protoner som sin kärna attraherar elektroner och det sätt på vilket de marginella "valenselektroner" elektroner ordna sig runt kärnan och andra elektroner.. Potatisen juice har utspädd fosforsyra, av vilka upplöser dissocieras till som väte katjoner (i grund och botten) och anjoner fosfat.
- 3Placera en galvaniserad spik i varje potatis.
- 4Placera en spik eller wire bit in i varje potatis säkerställer att spikarna inte röra. I detta skede är det verkligen viktigt att förstå att detta experiment kommer endast att fungera om galvaniserade spikar och naglar koppar / tråd är så långt ifrån varandra som möjligt på potatisen eftersom avståndet mellan dem är vad som ger makt.
- 5Ta bort batteriluckan från klockan. Om det redan finns ett batteri i den, ta bort den. Ta notis om batteriets polaritet i förhållande till hur den ansluter till klockan.
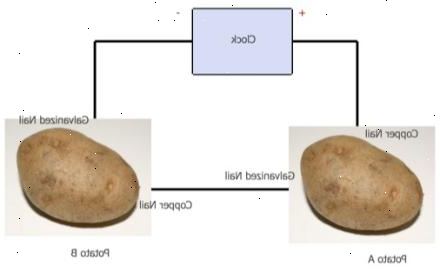
- 6Anslut den första bygel från koppar spik eller tråd av potatis A till den positiva polen av klockan. För att göra detta, ta en bygel bly och bifoga alligator klipp till koppar spik eller tråd och sedan den andra änden har krokodilklämmor till den positiva polen (betecknas med symbolen +).
- 7Anslut den andra bygel från den galvaniserade spiken av potatis-B till den negativa polen av klockan, betecknas med symbolen "-".
- När du håller den zinkelektroden (pläteringen på galvaniserad spik) och koppar elektrod (koppar spik eller tråd) i potatisen, varje metall, som har mindre elektronaffinitet än vätejoner, skulle tendera att ha sina atomer fråntagen sin elektroner av vätejoner. De neutrala väteatomer skulle gå samman i molekyler vätgas och fly, metallkatjonerna skulle tendera att skingra bort och mer väte diffunderar in för att fortsätta reaktionen långsamt bubblande bort syran är väte och tidskrävande metallerna.
- Zink har ännu mindre elektronaffinitet än koppar. Så, om du ansluter elektroderna med en ledare, tråd, kommer några elektroner tenderar att flyta i det från zink till koppar.
- Avlägsnandet av några elektroner från zinkelektroden kommer att göra några av sina atomer faller av som katjoner och lösas bort. Det överskott av elektroner på koppar kommer att göra vätgas företrädesvis ta dem där uppe, men också tenderar att göra koppar håller sina elektroner och inte vara rostiga (eller, mer exakt, förskjuta reaktionsjämvikten så att kopparjoner som faller utanför tenderar att återfå elektroner och sätta tillbaka för lite eller inget netto korrosion). Avlägsnandet av elektroner från koppar och tillsats av elektroner till zink skulle tendera att bygga upp områden av elektrisk laddning som skulle fördröja reaktionen. Men fler elektroner hålla ledande genom viran, och mer väte-och zinkjoner hålla dispergering genom potatisen att bibehålla färsk lösning vid varje elektrod, för att hålla reaktionen igång. Den kraft med vilken koppar sålunda drar elektronerna kan användas för att utföra arbete, som att köra en klocka..
- 8Anslut den tredje bygel till den galvaniserade spiken i potatis A. Anslut sedan den andra änden till koppar spiken i potatis B. Genom detta skede alla tre jumper kablar är sammankopplade och klockan ska fungera.
- 9Kontrollera klockan. Det bör nu vara igång på potatis makt.
- Reaktionen saktar som zinkmetall och vätejonerna är uttömda. Den kraft med vilken väte dras elektronerna utanför zink, i ett mycket omständligt sätt, är vad cellen gör tillgängliga för dig för arbete - med lite som "slöseri", förstås.
- Ledningar potatis cellerna end-to-end gör en "serie-krets", drar ström av elektroner genom klocka med dubbelt så mycket kraft som en potatis skulle gälla. Det gör dem också korrekt kallas en "batteri", eftersom du använder mer än en elektrokemisk "cell".
- När det fungerar, varför inte ställa in tiden på klockan till aktuell tid!
- Om klockan inte fungerar, kontrollera att alla anslutningar är säkra och i rätt ordning, och dubbelkolla polariteten på klockan. Om det fortfarande inte fungerar, kan din klocka kräver mer ström än väldigt lite en grönsak batteri kan ge. Du kan försäkra dig om att batteriet producerar några el med en och mäta spänning (elektrisk tryck) och ström (elektrisk flöde, ampere). Om du måste välja skalor, väljer mycket låga och kära: dessa batterier ger en volt eller två och några milliampere.
Tips
- Du kan köpa ett kit potatis klocka. Billigare har bara en klocka som ansluts till potatisen med sladdar och elektroder, dyrare håller potatisen i en integrerad enhet med koppar.
- Det är inte bara potatis du kan göra detta med. Prova andra frukter och grönsaker, till exempel citrusfrukter, avokado, bananer, etc. Det kommer även att arbeta i läsk.
- Israeliska forskare har funnit att de kan producera upp till 10 gånger den ström när potatisen kokas.
- En citrongul batteri fungerar ungefär på samma sätt, men med citronsyra i stället för fosforsyra tillhandahåller vätejoner. Andra typer av batterier kan likaledes dig att utnyttja energin i elektronernas flöde från ett område där de lättare får upp till där de lättare accepteras men skiljer sig i många detaljer.
- Fenomenet med de extra elektronerna hålla kopparn korroderar kan vara användbart också. Om det är ditt mål, du sa att använda "katodiskt skydd" snarare än att göra ett batteri. En billig bit av reaktiv metall, såsom zink eller magnesium, kan korrodera bort sig själv och fylla på elektroner för att skydda en värdefull struktur av mindre reaktiv metall, som en bro eller ett fartyg. (Vatten är inte alls lika reaktivt som batterisyra, så den reaktiva metallen varar ett tag, även med inget motstånd mot strömmen i ledaren.) För en stor struktur, kan man använda likström "påtryckt ström" från ett till- -plats generator eller nätspänning (med en professionellt utformad maskin - el och vatten kan vara farligt).
- Klockan är förmodligen en kvarts klocka, som gäller el till en liten kvarts kristall stämgaffel fysiskt "ringen" den vid sin resonansfrekvens. Gaffeln ger tillbaka en elektrisk signal med varje vibration. Övriga delar räknas elektroniskt vibrationerna, beräkna motsvarande tid, och ordna kristallerna i displayen för att visa det.
Varningar
- Små barn bör hållas under uppsikt när du utför detta experiment - naglar och ledningar är vassa och kan orsaka skada om de hanteras felaktigt. Borttagning av batterier bör också övervakas.
- Ät inte potatisen efteråt.
Saker du behöver
- 2 stora rena potatisar, eller 2 halvor av en stor potatis.
- 2 galvaniserad spik (zink)
- 2 koppar naglar eller trådar
- 3 jumper kablar (med krokodilklämmor i varje ände)
- Batteridriven LCD klocka (grå skärm med svarta siffror, som en billig klocka, som normalt tar bara ett 1.5V batteri)
